Stål er vår tids mest anvendte materiale. Dessverre har det et stort minus, det ruster, korroderer, ganske raskt. Det er derfor av stor betydning å beskytte stål mot korrosjon.
Den beste korrosjonsbeskyttelsen oppnås med zink. Zinkbelegg beskytter stål mot korrosjon på to måter.
• Ved barrierevirkning, i.e. ved å hindre oksygen og fuktighet i å trenge inn til ståloverflaten.
• Ved å gi katodisk beskyttelse i riper, slagmerker klippkanter o.s.v.
Zink er et uedelt metall med stor korrosjonstilbøyelighet. At det allikevel korroderer lite i de fleste miljøer beror på at zinkoverflaten raskt dekkes av fast-sittende korrosjonsprodukter som hindrer videre angrep.
Korrosjon i atmosfæren
Når en varmforzinket gjenstand trekkes opp av zinkbadet angripes overflaten umiddelbart av luftens oksygen, og et sjikt av zinkoksid dannes på overflaten. Ved videre reaksjon med luftens innhold av fuktighet og karbondioksid dannes basiske zinkkarbonater. Disse gir et tett sjikt med god vedheft. Karbonatene er tungt løselige i vann og gir meget god beskyttelse for zinkoverflaten (15). Luft inneholder også svoveldioksider som omdanner de basiske zinkkarbonater til mer lettløselig zink-sulfat og -sulfitt. Luftens innhold av svoveldioksid er imidlertid kraftig redusert i de senere år (bilde 1-2), og derved også den atmosfæriske korrosjon på zink.
Atmosfærens innhold av svoveldioksid påvirker altså korrosjonshastigheten. I industriatmosfære er derfor korrosjonen større enn i by- og landsbygdmiljø. Av betydning for korrosjonshastighet er også eksponeringsvinkelen. Korrosjonen er kraftigere på en horisontal flate enn på en vertikal. Flater i le korroderer også mindre.
Zinkbelegg som eksponeres i atmosfæren blir etter noen måneder matte og lysegrå. (bilde 1).
I marin atmosfære påvirkes angrepet på zink av luftens saltinnhold. I den marine luften finnes også mindre mengder av magnesiumsalter som har en passiverende effekt. Korrosjonen er derfor ikke så stor som man kunne forvente. Saltinnholdet avtar også raskt fra strandsonen.
Mange faktorer
Zinks korrosjon påvirkes av mange faktorer. Det er derfor ikke mulig å angi en allmenngyldig formel for korrosjonshastighet. Zinkbelegg har vært brukt for korrosjonsbeskyttelse av stål under svært forskjellige forhold i lang tid, med utmerket resultat. Kjennskapet til zinks korrosjonsbestandighet i ulike miljøer er derfor svært god. Det finnes mange eksempler på zinkbeleg som er eksponert i over hundre år.
Rødbrun missfarging
Silisiumtettede stål, som har en stor andel av jern-zink fase i belegget, kan etter en tids eksponering få en rødbrun fargetone som mørkner med tiden. Jern-zink fasen korroderer, hvorved jern frigjøres, som sammen med luftfuktighet danner jernoksid, rust. Jernoksidet har en kraftig farge, og selv små mengder kan gi kraftig missfarging (bilde 2).
En slik kraftig missfarging kan tas som tegn på at korrosjonsbeskyttelsen er kraftig nedsatt eller borte. Dette er imidlertid sjelden tilfelle. Jernzink legeringen kan ha ca. 30 % bedre korrosjonsbestandighet enn ren zink .
Om estetiske forhold krever det kan en missfarget flate overmales. En rødbrun lyktestolpe hadde etter 30 års eksponering ennå 70 µm zinkbelegg, tilstrekkelig beskyttelse for nok 50 års eksponering.

Bilde 1. Eksponert zinkbelegg med et ytre lag av ren zink. Overrflaten dekkes av grå korrosjonsprodukter, også kalt zinkpatina.

Bilde 2.Rødbrun missfarging.
Korrosjon i væsker
Slik som i luft får zinkbelegg i væsker også beskyttende belegg av korrosjons-produkter. Væsker kan være sure eller alkaliske og inneholde løste eller faste aggressive stoffer. Væskens temperatur og strømningshastighet er også av stor betydning. Dette betyr at beskyttelses-sjiktet kan få høyst varierende sammensetning, eller ikke dannes i det hele tatt.
Den elektrokjemiske korrosjonen som i luft har liten betydning, har stor betydning i væsker. Avhengig av væskens elektriske ledningsevne skjer den elektrokjemiske korrosjon, og oppbygging av beskyttelses-sjikt, over større eller mindre områder.
Størst betydning har væskens pH-verdi. Zinks korrosjonshastighet er relativt lav og stabil i pH-området 5,5 – 12,5 ved temperaturer mellom 0-20°C.
Hardt vann, som inneholder kalk og magnesium, er lite aggressive. Disse elementer danner, sammen med karbondioksid, tungt løselige karbonater, og gir stabile beskyttelsessjikt.
Bløtt vann har lite salter, danner ikke beskyttelsessjikt, og er aggressivt overfor zink. Det kan også, av og til, forekomme at det skjer en polaritetsveksling mellom zink og stål slik at stål blir anode (oppløsningspol) i elementet. Dette gir risiko for punktkorrosjon. Polaritetsveksling motvirkes av karbondioksid, sulfater og klorider, og skjer derfor ikke i f.eks. sjøvann, men kan forekomme i meget rent vann.
Aggressivt, bløtt vann finns i en del vassdrag og innsjøer i Finland, Norge, og Sverige. Har vannet raskere strømningshastighet enn 0,5 m/s dannes ikke beskyttelsessjikt, og korrosjonshastigheten øker.
Vanntemperaturen har også stor betydning for korrosjonshastigheten. Over ca. 55°C får de beskyttende korrosjonsproduktene en grovkornet struktur og dårlig vedheft til zinkoverflaten. De faller lett av, og blottlegger ny, frisk zink for nye angrep.
Korrosjonshastigheten når et maksimum ved ca. 70°C, for så å synke til den ved 100°C er av samme størrelsesorden som ved 50°C.
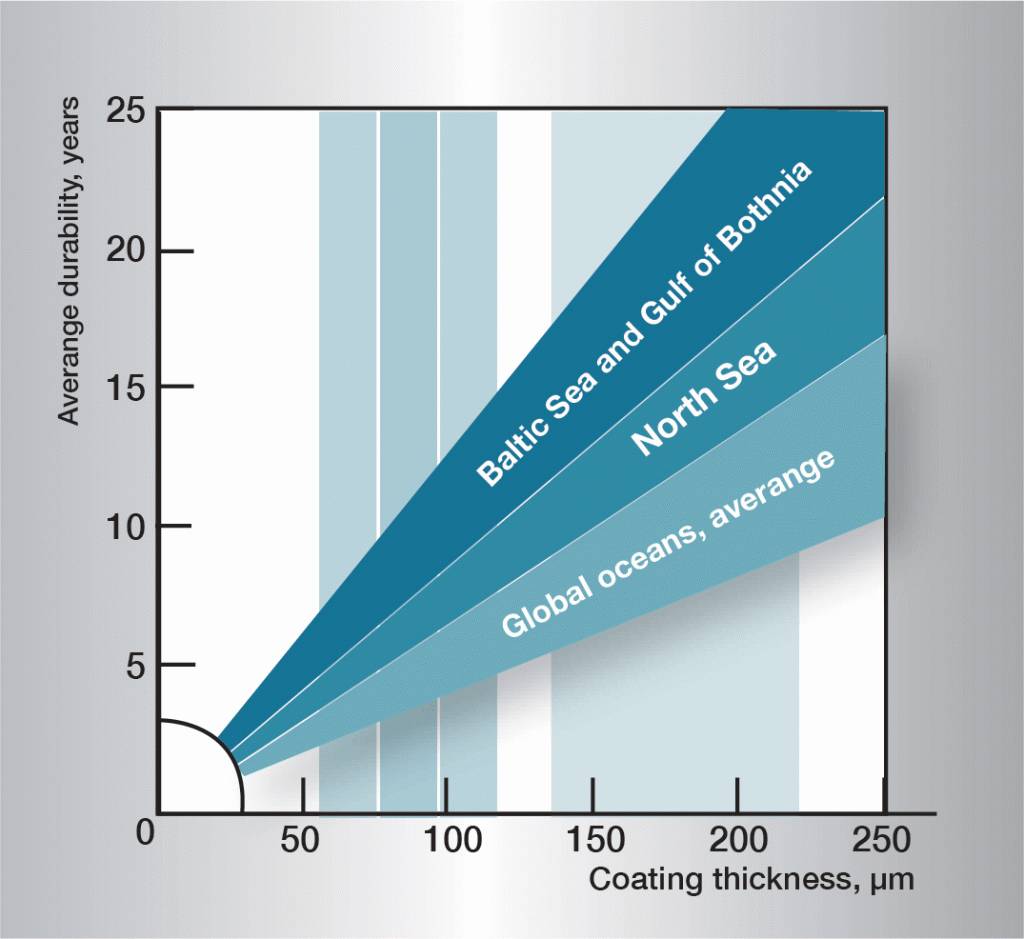
Som man ser av det foregående er korrosjonforløpet i vann meget komplisert, og det er vanskelig å gi noen allmenngyldige regler. Det er imidlertid mange praktiske erfaringsdata, og bilde 3 gir retningsverdier for noen vanntyper.
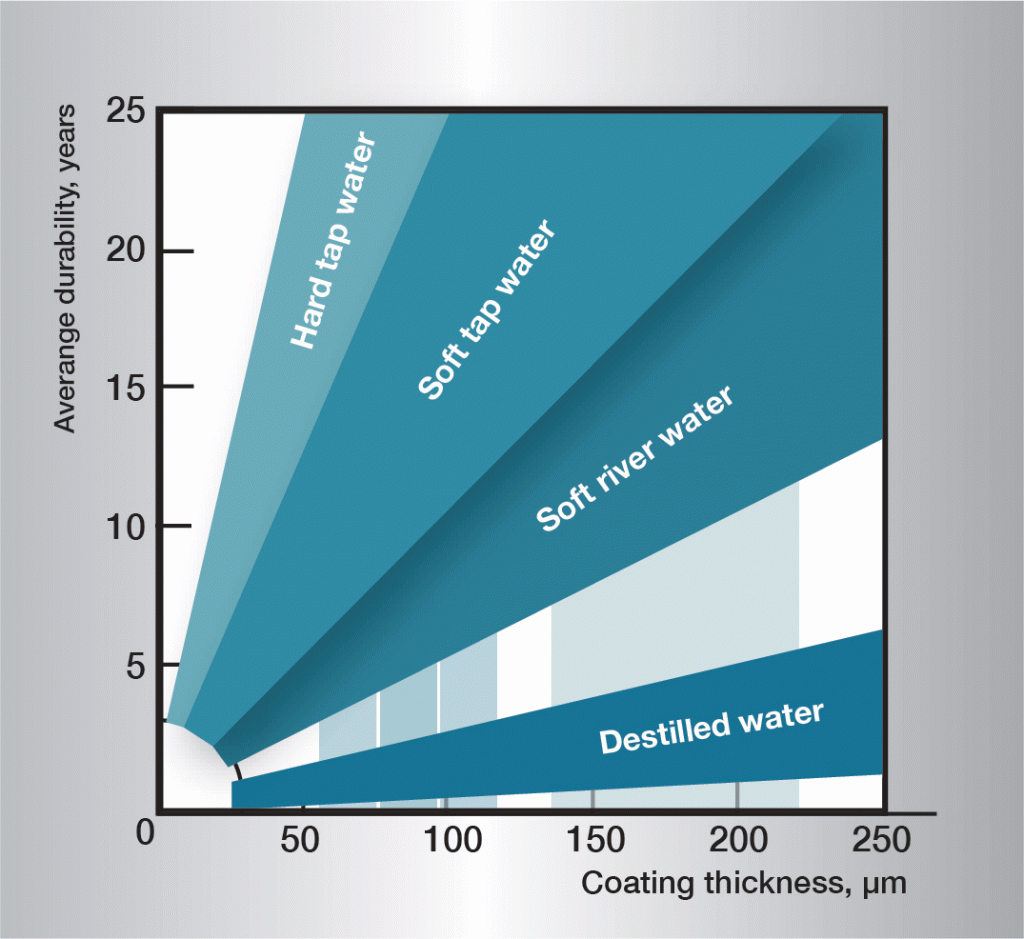
Bilde 3. Gjennomsnittlig levetid for zinkbelegg i ulike vanntyper.
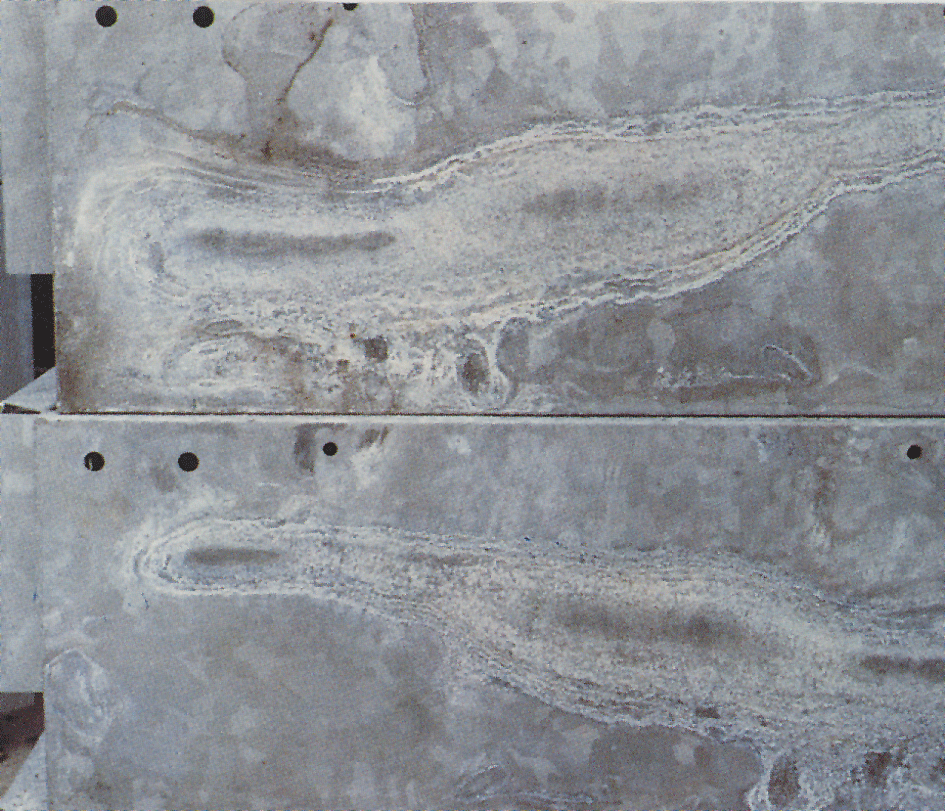
Hvitrust
Fra tid til annen dannes et hvitt, melaktig, og voluminøst belegg på zink og zinkbelegg. Dette kalles hvitrust (bilde 4). Hvitrust dannes på nyforzinket gods når dette utsettes for regnvann eller kondens. Dette kan skje i spalter, f.eks. mellom tett sammenlagt gods. Flater hvor det er god lufttilgang, og det normale beskyttelses-sjiktet er bygd opp, angripes sjelden. Angrepet stopper altså opp, eller hindres, ved fri lufttilgang. Gjensittende hvitrust forsvinner etter hvert. Zinkflaten får igjen et normalt, varmforzinket utseende.
Hvitrust er meget voluminøst, ca 500 ganger større enn den zink det dannes fra. Et angrep kan derfor se meget alvorlig ut. Som oftest har imidlertid et hvitrust angrep liten eller ingen betydning for et varm-forzinket beleggs levetid.
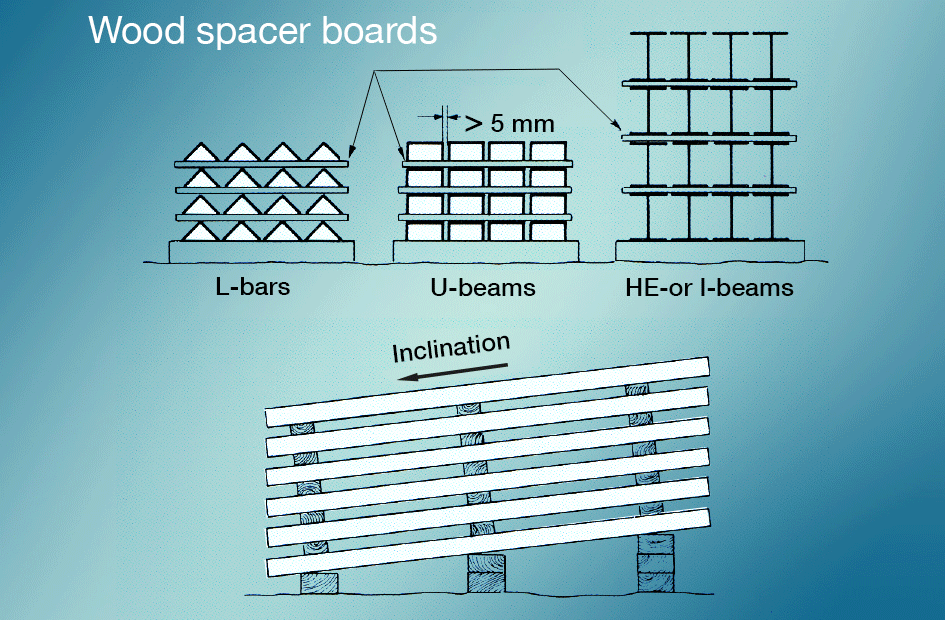
Hvitrust unngås best ved at nyforzinkede gjenstander hindres i å komme i kontakt med kondens eller regnvann under lagring og transport. Problemet kan unngås ved at godset lagres under tak noen dager, eller at det legges opp slik at vann kan renne av, og at det er fri lufttilgang fra alle sider. (Bilde 10-5).
Allerede dannet hvitrust kan fjernes med forsiktig mekanisk eller kjemisk behandling. Etter varmforzinkings-standarden er hvitrust ikke reklamasjonsårsak.
Korrosion i jord
Korrosjonsforholdene i jord er meget kompliserte, og variasjonene kan være meget store fra sted til sted, selv ganske nær hverandre. En antydning om forskjellige jordarters korrosivitet er gitt i bilde 6.
For å bestemme jordkorrosivitet kan måling av jordartens elektriske motstand (resistivitet) brukes. Bilde 7 gir en indikasjon på ulike jordarters aggressivitet. Ved bruk av metaller, og forzinket gods, i jord, bør lokal ekspertise rådspørres.

Galvanisk korrosjon

Kobles to ulike metaller eller legeringer sammen i nærvær av en elektrolytt, dannes et galvanisk element, en galvanisk celle. Hvilket av metallene som blir anode eller katode bestemmes av deres elektrodepotential i den aktuelle elektrolytt. I sjøvann, som gjelder for de fleste praktiske tilfeller, er de forskjellige metaller og legeringers plass i den galvaniske spenningsrekke som vist i bilde 7.
Galvanisk korrosjon kalles også bimetallkorrosjon. Denne effekt benyttes til ”katodisk beskyttelse” av konstruksjoner i vann og andre elektrisk ledende medier.
Zinkbeleggs katodiske beskyttelseseffekt
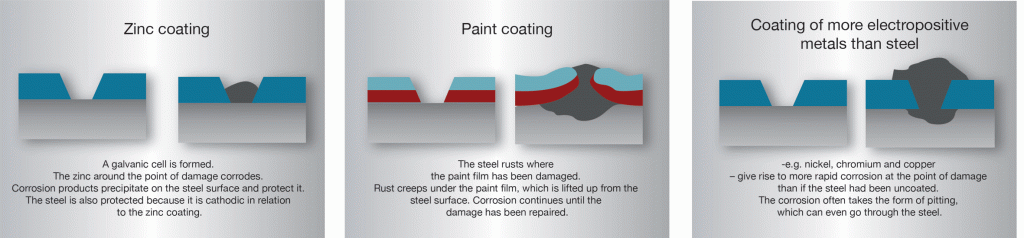
I varmforzinket gods har zink og stål god elektrisk kontakt. Ved skade i zinkbelegget dannes en galvanisk celle dersom det er fuktighet, en elektrolytt, tilstede. I denne cellen blir zink anode (oppløsningspol), og korroderer, mens stålet blir katode, og beskyttes.
På grunn av den katodiske beskyttelsen zinken gir, kan ikke rust krype under belegget der det oppstår skader. Dette i motsetning til hva som skjer ved malingsbelegg og belegg av edlere metall.
Zinkbelegg på stål er således unike i den betydning at en mindre skade i belegget ikke medfører noen vesentlig reduksjon av beskyttelsen.
I startfasen kan man se en svak rustdannelse på den blottlagte flate. Denne dekkes etter hvert av tungtløslige korrosjonsprodukter fra zinken som beskytter mot videre angrep). Dette kalles ofte for en selvlegende prosess hvilket ikke er riktig da zinkbelegget i seg selv ikke utbedres.
Galvanisk korrosjon på forzinket stål i kontakt med innstøpt armering
Dersom varmforzinket stål kommer i kontakt med armeringsstål innstøpt i betong, og en elektrolytt er i kontakt med det varmforzinkede stålet, kan det dannes en galvanisk korrosjonscelle. Dette forhold er observert både i veianlegg når varmforzinkede stolper har kommet i kontakt med broarmering, og i fjøsbygninger hvor det er laget kontakt for å potentialutligne bygningen.
Når vanlig armeringsjern av karbonstål støpes inn i betong blir det passivert (edelt), hvilket innebærer at det får et korrosjonspotential tilsvarende rustfritt stål. Dersom fjøsinnredningen, som vanligvis er varmforzinket, kommer i kontakt med den innstøpte armeringen, dannes det en galvanisk celle som kan gi meget rask korrosjon av zinkbelegget.
Når zinken har korrodert bort, fortsetter angrepet på det underliggende stålet, og kan medføre at konstruksjonen bryter sammen. Årsaken er at stålet her har et korrosjonspotential som er betydelig mer negativt (uedelt) i væske, gjødsel eller fuktig strø, sammenlignet med korrosjonspotentialet for innstøpt stål, som passiveres. Til tross for at det er samme type stål, gjør de ulike miljøer som materialet brukes i at det innstøpte stålet blir katode, og det fukteksponerte, anode i den galvaniske cellen.
Ved galvanisk korrosjon er også størrelsen på katoden (edelt metall), og anoden (uedelt metall) av stor betydning. I dette tilfelle har armeringsmatten (katoden) en stor overflate i forhold til det varmforzinkede stålet der anodeflaten kun består av lokale, mindre, felter der elektrolytten er i kontakt med metallet. Dette uheldige størrelsesforholdet akselererer korrosjonen.
Korrosjonsangrepene skjer for eksempel på innredningsdetaljer i båsenes nedre deler som utsettes for urin og gjødsel, eller ved drikkekoppene. Hvor raskt korrosjonen skjer, beror på en rekke ulike faktorer. Sammenhengen mellom tørr- og våttid for utsatte overflater, typer av strømiddel, innredningssystem, båser / løsdrift, påvirker korrosjonsforløpet. Normalt vil et strømiddel med høy oppsugningsevne gi et tørrere miljø, og mindre fare for økt korrosjon.
Zinkbelegg i kontakt med andre metaller
Som det fremgår av bilde 7 er zink mindre edelt enn de fleste bruksmetaller. Dette betyr at zink blir anode, oppløsningspol, og korroderer, dersom det står i elektrisk kontakt med et mer edelt metall. Slike sammenkoblinger bør derfor unngås, f.eks. ved å bruke isolerende mellomlegg. I luft, og normalt tørre omgivelser, gir sammenkobling av zink – zinkbelegg, og aluminium eller rusfritt stål ingen merkbar korrosjon. Katodeflaten må ikke bli for stor i forhold til anodeflaten. I vann skal det alltid brukes isolerende mellomlegg.
Kobber og kobberlegeringer er mer elektrisk aktive, og det forekommer at kobberioner løses ut, og dette kan gi store angrep. Kobber og kobberlegeringer må alltid isoleres fra zink og zinkbelegg.
Pakking og transport av varmforzinket gods
Selv om belegget på varmforzinket gods tåler hard behandling bør det vid lagring og levering behandles med fornuft. Enkel pakking og bunting gir beskyttelse mot mekaniske skader, samt transporttekniske fordeler.
Pakking og bunting må gjøres luftig, og om nødvendig med mellomlegg, slik at hvitrust dannelse ikke skjer.
